
NEWS
新闻中心
SERVERS
服务项目
NEWS
最新资讯
发布时间:2024-04-26
大脑,是人体内的星系。当前,脑卒中、脑肿瘤、脑积水、帕金森病、癫痫病、阿尔茨海默病、脑炎等脑部疾病,已成为难以回避的社会问题。数据显示,全球目前约有10亿人口患有脑疾病,占全球所有疾病负担的28%,也是全球第二大死亡来源。

斑马鱼,是研究人类脑疾病的理想模型,其与人类基因同源性高达87%,绝大部分遗传疾病可在斑马鱼中建模,并具有胚胎透明、易于观察、大脑结构相对简单、神经元数量适中等显著优势,便于进行大规模的遗传学和表型学研究,并可靠模拟脑疾病的发生和发展过程。近年来,随着斑马鱼及基因编辑技术的快速发展,斑马鱼与基因编辑在脑科学研究中的应用越来越广泛,为我们更深入地理解大脑的功能和机制,开发新的治疗方法提供了新的视角和方法,并呈现出巨大的应用潜力。
01、斑马鱼基因保守性及转录学分析
当前,斑马鱼因其高度的基因保守性和独特的转录学特性,在脑科学研究中具有不可替代的地位。
斑马鱼神经系统与人体的相似性
斑马鱼大脑系统的主要结构与哺乳动物相似,在生理学、脑解剖学和神经化学方面都与人类的特征基本相同,其神经递质系统,包括胆碱能、多巴胺能、去甲肾上腺素能通路已经被阐明,其基因表达、细胞信号传导等过程也与人类相近;
与人类相当的行为,如运动活动、焦虑样行为、学习、记忆保留、空间和物体识别、恐惧反应、社会偏好和互动等,都能在斑马鱼身上得到体现。研究表明,硬骨鱼的侧脑皮层与哺乳动物海马相似,能够获得和记忆空间信息;内侧大脑皮层功能在某种程度上与哺乳动物的杏仁核(恐惧和其他情绪的中心)相似。因此,斑马鱼幼体不仅表现出短期记忆,而且还表现出长期记忆及联想和社会学习性,是研究学习和记忆的生物机制的最佳模式生物之一。
斑马鱼白天很活跃,在视觉、听觉和嗅觉功能方面具有生理优势;脑血屏障(BBB)在3dpf-10dpf发育;可以通过基因编辑、药物诱导或化学诱导产生类似于人类CNS的疾病模型,通过行为测试和社会学分析模拟人类,结合荧光标记、电生理生物化学、神经化学、组学、分子分析等方法,建立高通量分析,实现整体动物光学可视化和高通量筛选。
斑马鱼基因保守性分析
斑马鱼基因保守性主要体现在与人类和其他脊椎动物基因的相似性上,包括与神经系统、免疫系统、代谢系统等相关基因。斑马鱼基因组与人类相似性高达87%以上,绝大部分遗传疾病可在斑马鱼中建模,为利用斑马鱼研究人类疾病提供了坚实的基础。

斑马鱼基因保守性还体现在其功能和调控机制上,为更好地了解人类基因功能和调控机制、疾病的预防和治疗提供了新的思路和方法。许多在斑马鱼中发现的基因和分子机制在人类中同样存在,并发挥着相似功能。如,斑马鱼Sec13基因与人类Sec13基因在进化上高度保守,其功能和调控机制都涉及到内质网到高尔基体的转运过程;斑马鱼rictor基因也与人、小鼠等的rictor基因相似性很高,在调节细胞生长、增殖和代谢等方面发挥着重要作用。
斑马鱼转录组学分析
通过高通量测序技术对斑马鱼进行转录组学分析,不仅可以获取斑马鱼各组织、器官或细胞类型的转录组数据,包括mRNA、非编码RNA等多种类型RNA,而且可以揭示斑马鱼在不同发育阶段、生理条件或环境变化下基因表达变化情况,有助于研究者更全面地了解斑马鱼基因表达情况,深入理解斑马鱼基因的功能、调控机制及疾病机制等;
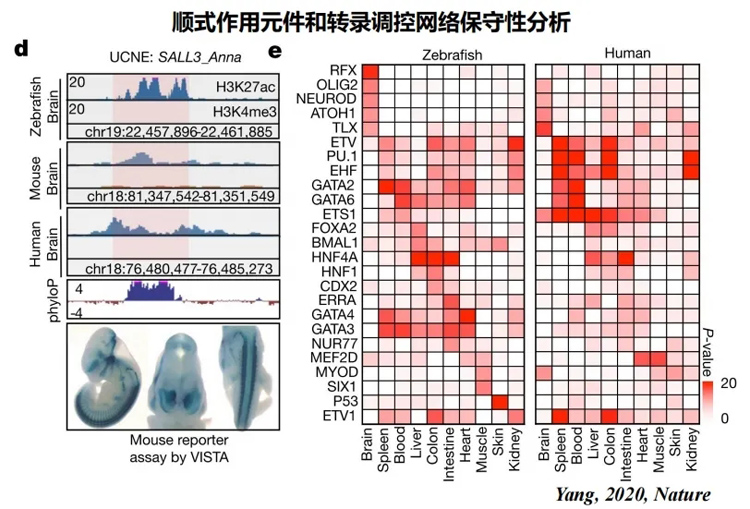
通过比较正常与疾病状态下的斑马鱼转录组数据,可以发现与疾病相关的差异表达基因,为疾病诊断、治疗提供新的靶点和思路,也可以基于斑马鱼基因表达的变化情况,来预测人类疾病发生风险,丰富对斑马鱼基因组的认知,为后续研究提供新的方向。
02、斑马鱼与基因编辑在脑科学研究的应用
近年来,斑马鱼与基因编辑技术,为脑神经发育研究、神经退行性疾病研究、药物筛选与毒性测试及脑科学研究提供了强大的工具,基因表达数据库和斑马鱼大脑图谱也可用于探索与神经精神疾病相关的大脑区域的基因组学和神经解剖学研究。
通过精确地修改斑马鱼基因组中的特定基因,标记特定的器官与组织细胞,进行直观、可视化展示与动态观察,不仅可以研究基因的功能与表达模式,探究基因在脑神经发育、功能及疾病发生中的作用,而且可以研究基因与疾病的关系,建立基因编辑疾病模型,以模拟人类神经退行性疾病、精神疾病等的病理过程,从而深入探究疾病发病机制,还可以开展遗传病/罕见病致病基因确认与机制研究、新靶点新通路新标志物的确认与验证等。
用于活体神经系统研究及标记
在活体神经系统研究中,斑马鱼基因编辑技术为活体神经系统研究及标记提供了前所未有的机会。利用转基因方法,可以构建标记特定神经元斑马鱼品系;利用融合荧光蛋白的方法,可以标记并监测特定蛋白的动态变化。
通过荧光标记或激光共聚焦钙成像等技术,活体标记各种类型的神经元和神经系统相关分子、活体电活动记录神经元中钙离子成像等,从而实时观察神经元的活动、连接及信号传递过程,有助于深入了解神经系统的结构、功能及运行机制,为神经退行性疾病、精神疾病等的防治提供新的思路和方法。
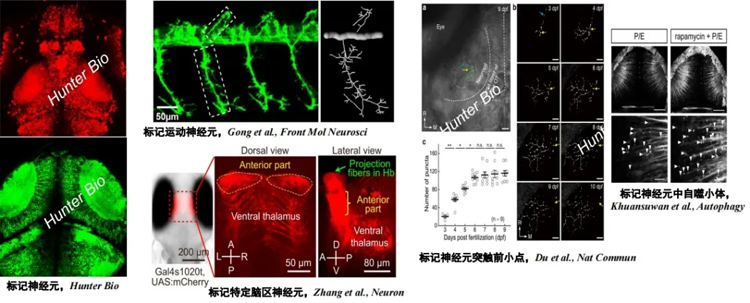
图为活体标记-各种类型的神经元和神经系统相关分子
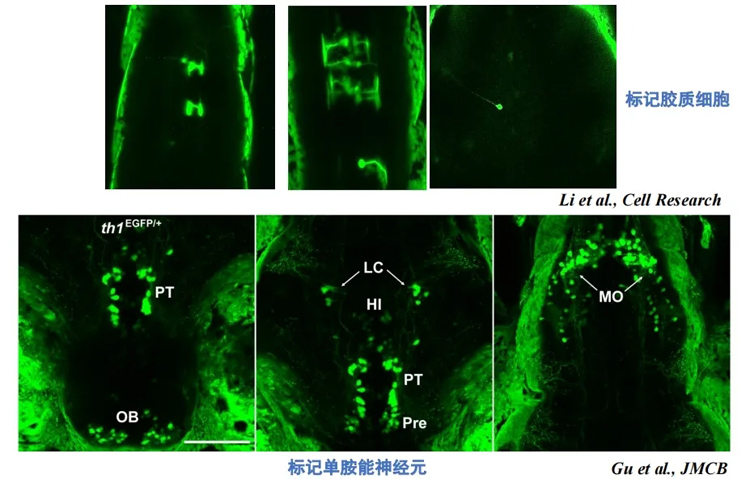
图为基因编辑技术助力活体神经系统研究:敲入实现标记
用于脑神经发育研究
利用斑马鱼基因编辑技术,研究人员可以敲除或突变斑马鱼中参与脑神经发育的关键基因,观察这些变化对神经系统结构和功能的影响,从而揭示脑神经发育的分子机制和调控网络。
以“帕米帕利引起斑马鱼胚胎神经发育缺陷和脑出血的分子机制”这一研究为例,该研究以斑马鱼为研究对象,首次发现Pamiparib会引起斑马鱼胚胎脑发育异常和脑出血,揭示了Pamiparib可通过抑制Notch信号通路诱导脑损伤的这一新的分子机制,研究为Pamiparib的作用机制和的安全使用提供了重要的研究思路。

图为Pamiparib诱发斑马鱼神经发育缺陷和脑出血
来源:“Pamiparib induces neurodevelopmental defects and cerebral haemorrhage in zebrafish embryos via inhibiting notch signaling”,《Molecular Neurobiology》,2022年8月19日
用于神经退行性疾病模型构建及研究
当前,神经退行性疾病(NDs)随着预期寿命的增加而恶化,如阿尔茨海默病(AD)、帕金森病(PD)、肌萎缩性侧索硬化症(ALS)和亨廷顿病(HD)等,这些疾病的共同特征包括特定神经元的选择性神经退行性变。
目前,环特生物已构建了多种神经退行性疾病模型。通过模拟人类神经退行性疾病相关的基因突变,研究人员可以在斑马鱼中创建疾病模型,研究疾病的发病过程和机制,不仅有助于理解疾病的本质,还为开发新的治疗策略提供了线索。
以肌萎性侧索硬化症(ALS)模型构建为例,ALS 是一种进行性神经退行性疾病,表现为肌无力、反射亢进、面部化、萎缩、痉挛,最终导致瘫痪,其病理特征是皮层的上运动神经元或脊髓和脑干的下运动神经元进行性丧失。目前尚无针对该病的有效治疗方法,患者主要表现为运动神经元疾病的严重骨骼肌无力。
常见的肌萎性侧索硬化症(ALS)模型构建方法包括基因编辑、神经毒素诱导、金属离子诱导等,如下图所示:

2024年3月2日,Umeå大学的一项关于肌肉萎缩症的最新研究中,研究人员创建了斑马鱼肌肉萎缩症疾病模型,并使用基因编辑技术来研究肌肉萎缩症如何影响眼部肌肉,通过转录组分析证明了斑马鱼EOMs和躯干肌肉对肌肉营养不良反应的基因表达的重要差异,同时证明了Fhl2是一种保护因子,是治疗肌营养不良症的候选靶基因。

以亨廷顿舞蹈症(HD)为例,同样作为一种遗传性神经退行性疾病,其特征是舞蹈病(称为舞蹈病)的多动运动障碍,伴有痴呆、行为和精神障碍。它是由亨廷顿基因(HTT)外显子1的显性遗传CAG重复扩增引起的。 HTT的突变导致突变蛋白在大脑中的积累,这些突变蛋白主要聚集在纹状体中。随着疾病的进展,患者逐渐失去说话和移动的能力,伴有认知能力下降。
常见的亨廷顿舞蹈症(HD)模型构建方法包括基因编辑、药物诱导等,如下图所示:

用于精神疾病或遗传脑疾病模型构建及研究
当前,急性和慢性压力源是人类精神疾病的常见诱因,常见的与压力相关的精神障碍包括双相情感障碍、抑郁症、焦虑症、精神分裂症和创伤后应激障碍(PTSD)等,这些疾病源于神经内分泌、神经递质和神经免疫系统的紊乱。
与此同时,由遗传因素所致的代谢性脑病也居高不下,包括溶酶体贮积病、过氧化物酶体病(ALD)、线粒体病(Leigh病、MELAS、KSS)、原发性脑白质病(脑白质营养不良) (Canavan病、亚历山大病、半乳糖血症、肌酸缺乏症)。
近年来,斑马鱼与基因编辑技术在精神疾病或遗传性脑疾病模型构建、发病机制研究及药物筛选等方面发挥重要的作用。目前,环特生物已构建了多种精神疾病或遗传脑疾病模型。
在精神疾病模型构建方面,通过模拟人类精神分裂症相关的基因突变,可以在斑马鱼中构建精神分裂症模型,进而观察其脑部在病理状态下的活动变化。由于斑马鱼的行为相对丰富,如群聚行为,这种典型的社交行为可以在一定程度上反映斑马鱼的认知状况,从而为研究精神分裂症提供新的视角。
以自闭症(ASD)模型构建为例,它是由神经发育缺陷引起的,属于影响全球约2%的人的主要人格障碍类型之一,其中大多数是儿童或青少年。成功的生物体模型是破译中枢神经系统与自闭症之间关系的关键。通过在啮齿动物和人类中进行研究,已经确定了各种ASD相关基因。常见的自闭症(ASD)模型构建方法包括基因编辑、药物诱导、金属离子诱导等,如下图所示:

在遗传脑疾病模型构建方面,斑马鱼的遗传相似性使其成为研究人类遗传脑疾病的理想模型。研究人员可以利用斑马鱼来模拟人类遗传脑病相关基因突变,通过研究疾病发病机制、生理学变化和潜在治疗策略,从而更深入地了解遗传脑疾病的发生发展过程,为脑疾病的预防和治疗提供理论依据。
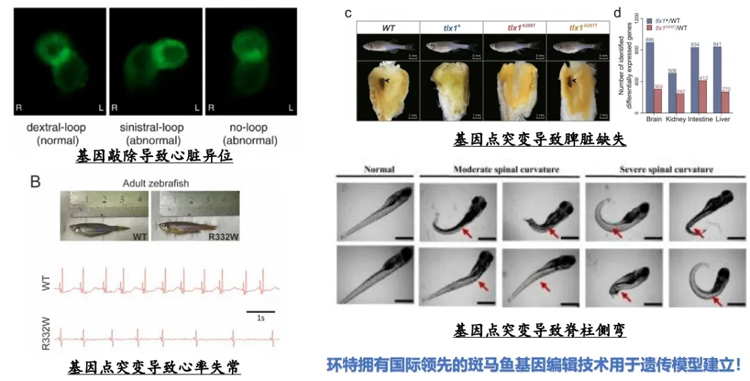
用于神经系统药物筛选与毒性测试
利用斑马鱼模型,研究人员可以快速评估药物对神经系统的影响,筛选出具有潜在疗效的药物,还可以用于评估药物的神经毒性,为药物的安全性评估提供重要依据。
在最近的一项研究中,一种突变的mtdp-43斑马鱼发现了亚甲蓝(mb)的治疗潜力,这是通过分析各种化合物改善肌萎缩侧索硬化(ALS)样表型的疗效发现的。同样,mtdp-43突变斑马鱼存在短的、异常分支的运动轴突,氧化应激增加,逃逸反应异常。给予MB(一种神经保护剂)可以纠正游动和轴突表型,同时减少由于未折叠突变蛋白积聚而产生的内质网(ER)应激。在G93A-mtsod1转基因小鼠模型中,将ER应激作为ALS药物治疗的潜在靶点,促使进一步测试几种相关药物的疗效,从而确定和重新定位经批准的高血压药物gunabenz,作为ALS的潜在新治疗。
再以PTZ为例,PTZ是啮齿动物和斑马鱼中最广泛使用的惊厥药之一,能产生大量已知抗癫痫药物不同程度抑制的强效癫痫表现型。小分子筛选最早可在2 dpf时在斑马鱼身上进行,潜在的治疗效果不仅通过行为测试进行评估,还通过监测神经反应进行评估。暴露于PTZ会增加c-fos的表达,而c-fos的表达会被典型的抗惊厥药、抗炎药、天然和合成类固醇、抗氧化剂、血管扩张剂减弱。
近年来,斑马鱼+基因编辑技术的发展,为脑科学研究提供了越来越多的可能性。环特生物依托于斑马鱼+哺乳动物+类器官+基因编辑4大技术平台,基于过去10余年持续的技术创新实践,以专业、前沿的技术服务解决方案,助力脑科学研究与突破,共同探索更多未知中的微光,点亮生命之光!
业务合作咨询:成先生 173 6453 1293(微信同号)
